Hélio

Tabela Periódica
O hélio é um gás incolor e inodoro, monoatômico em condições normais de pressão e temperatura, tornando-se líquido somente em condições extremas (de alta pressão e baixa temperatura). À temperatura ambiente, o hélio encontra-se no estado gasoso. O hélio (gr. helios, Sol) é um elemento químico de símbolo He e que possui massa atômica igual a 4 u, apresentando número atômico 2 (2 prótons e 2 elétrons). Apesar da sua configuração eletrônica ser 1s2, o hélio não figura na tabela periódica dos elementos junto com o hidrogênio no bloco s, está colocado no grupo 18 (8A ou 0) do bloco p, já que apresenta nível de energia completo, apresentando as propriedades de um gás nobre, ou seja, é inerte (não reage) como os demais elementos.

O hélio é usado nos dirigíveis.
Tem o ponto de solidificação mais baixo de todos os elementos químicos, sendo o único líquido que não pode solidificar-se baixando a temperatura à pressão normal, já que permanece no estado líquido no zero absoluto. O hélio sólido só existe a pressões da ordem de 100 MPa a 15 K (-248,15 ºC). Aproximadamente a essa temperatura, o hélio sofre uma transformação cristalina, de estrutura cúbica a estrutura hexagonal compacta; em condições mais extremas, ocorre uma nova mudança, empacotando os átomos numa estrutura cúbica centrada. Todos estes empacotamentos tem energias e densidades semelhantes, debitando-se as mudanças à maneira como os átomos interagem.
O hélio tem o menor ponto de evaporação de todos os elementos químicos, e só pode ser solidificado sob pressões muito grandes. É o segundo elemento químico em abundância no universo, atrás do hidrogênio, mas na atmosfera terrestre encontram-se apenas traços, provenientes da desintegração de alguns elementos. Em alguns depósitos naturais de gás é encontrado em quantidade suficiente para a sua exploração; usado para o enchimento de balões e dirigíveis, como líquido refrigerante de materiais supercondutores criogênicos e como gás engarrafado utilizado em mergulhos de grande profundidade.
De resto, sua temperatura crítica é de apenas 5,19 K. Os isótopos 3He e 4He são os únicos em que é possível, aumentando a pressão, reduzir o volume mais de 30%. O calor específico do gás hélio é muito elevado, de vapor muito denso, expandindo-se rapidamente quando é aquecido a temperatura ambiente.
| Características | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome, símbolo, número | Hélio, He, 2 | ||||||||||||||||||||||||
| Classe , série química | Gás nobre , gás nobre | ||||||||||||||||||||||||
| Grupo, período, bloco | 18 (VIIIA ou 0), 1, s | ||||||||||||||||||||||||
| Densidade, Dureza | 0,1785 kg/m³, não apresenta | ||||||||||||||||||||||||
| Aparência e Cor | incolor |
||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||
| Configuração eletrônica | 1s2 | ||||||||||||||||||||||||
| Estado de oxidação (óxido) | 0 (desconhecido) | ||||||||||||||||||||||||
| Estrutura cristalina | hexagonal | ||||||||||||||||||||||||
| Massa atômica | 4,002602(2) u | ||||||||||||||||||||||||
| Raio atômico (calculado) | sem dados (31) pm | ||||||||||||||||||||||||
| Raio covalente | 32 pm | ||||||||||||||||||||||||
| Raio de van der Waals | 140 pm | ||||||||||||||||||||||||
| Elétrons por nível de energia | 2 | ||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||
| Entalpia de vaporização | 0,0845 kJ/mol | ||||||||||||||||||||||||
| Entalpia de fusão | 5,23 kJ/mol | ||||||||||||||||||||||||
| Pressão de vapor | inaplicável | ||||||||||||||||||||||||
| Velocidade do som | 970 m/s a 293,15 K | ||||||||||||||||||||||||
| Estado da matéria | gasoso | ||||||||||||||||||||||||
| Volume molar | 21,0 ×10-6 m³/mol | ||||||||||||||||||||||||
| Ponto de fusão | 0,95 K a 26 atm | ||||||||||||||||||||||||
| Ponto de ebulição | 4,22 K | ||||||||||||||||||||||||
| Informações diversas | |||||||||||||||||||||||||
| 1º Potencial de ionização | 2372,3 kJ/mol | ||||||||||||||||||||||||
| 2º Potencial de ionização | 5250,5 kJ/mol | ||||||||||||||||||||||||
| Calor específico | 5193 J/(kg*K) | ||||||||||||||||||||||||
| Eletro negatividade | sem dados (Escala de Pauling) | ||||||||||||||||||||||||
| Condutividade elétrica | sem dados | ||||||||||||||||||||||||
| Condutividade térmica | 0,152 W/(m*K) | ||||||||||||||||||||||||
| Isótopos mais estáveis | |||||||||||||||||||||||||
|
|||||||||||||||||||||||||
| Unidades SI e CNPT, exceto onde indicado o contrário | |||||||||||||||||||||||||
História
O hélio foi descoberto de forma independente pelo francês Pierre Janssen e pelo inglês Norman Lockyer, em 1868 ao analisarem o espectro da luz solar durante um eclipse solar ocorrido naquele ano, encontrando uma linha de emissão de um elemento desconhecido. Eduard Frankland confirmou os resultados de Janssen e propôs o nome helium para o novo elemento, em honra ao deus grego do sol (helios) com o sufixo -ium , já que se esperava que o novo elemento fosse metálico.

Imagem do Sol
Em 1895 Sir William Ramsay isolou o hélio descobrindo que não era metálico, entretanto o nome original foi conservado. Os químicos suecos Abraham Langlet e Per Teodor Cleve conseguiram também, na mesma época, isolar o elemento.
Em 1907 Ernest Rutherford e Thomas Royds demonstraram que as partículas alfa são núcleos de hélio.
Em 1908 o físico alemão Heike Kamerlingh Onnes produziu hélio líquido esfriando o gás até 0,9 K, o que lhe rendeu um prêmio Nobel. Em 1926 seu discípulo Willem Hendrik Keesom conseguiu pela primeira vez solidificar o hélio.
O hélio e suas aplicações
O hélio é mais leve que o ar, isto é, a densidade do hélio é menor que a densidade do ar, diferenciando-se do hidrogênio por não ser inflamável, entretanto, apresenta poder ascensional 8% menor. Por este motivo, e por ser um gás inerte, é utilizado em dirigíveis e balões com fins recreativos, publicitários, reconhecimento de terrenos, filmagens aéreas e para investigações das condições atmosféricas. As maiores reservas de Hélio encontram-se nos Estados Unidos. Estas reservas são estratégicas e controladas pelo governo norte americano. Não estão disponíveis para venda em grande quantidades.
Além das citadas o hélio tem outras aplicações, como:
- Em cromatografia de gases é usado como gás transportador inerte.
- A mistura hélio-oxigênio é usada para mergulhos a grande profundidade, já que é inerte e menos solúvel no sangue que o nitrogênio e se difunde 2,5 vezes mais depressa, reduzindo o tempo necessário para a descompressão, apesar de iniciar-se em maior profundidade elimina o risco de narcose por nitrogênio (embriaguês de profundidades).
- O hélio líquido encontra cada vez maior uso em aplicações médicas de imagem por ressonância magnética (RMI).
- Devido ao seu baixo ponto de liquefação e evaporação pode ser usado como refrigerante a temperaturas extremadamente baixas em imãs supercondutores e na investigação criogênica a temperaturas próximas do zero absoluto.
- A atmosfera inerte de hélio é empregada na soldadura por arco e na fabricação de cristais de silício e germânio, assim como para pressurizar combustíveis líquidos de foguetes.
- Em túneis de vento supersônicos.
- Como agente refrigerante em reatores nucleares.
Obtenção e Abundância
O hélio é o segundo elemento mais abundante do universo atrás apenas do hidrogênio e constitui em torno de 20% da matéria das estrelas, em cujo processo de fusão nuclear desempenha um importante papel. A abundância do hélio não pode ser explicada pela formação das estrelas, ainda que é consistente com o modelo do Big bang, acredita-se que a maior parte do hélio existente se formou nos três primeiros minutos do universo.
Na atmosfera terrestre existe na ordem de 5 ppm e encontrado também como produto de desintegração em diversos minerais radioativos de urânio e tório. Alem disso, está presente em algumas águas minerais, em gases vulcânicos, principalmente nos vulcões de lama e em certas acumulações comerciais de gás natural como nos Estados Unidos, Rússia e Argélia de onde provém a maioria do hélio comercial, associado ao gás metano.
Pode-se sintetizar o hélio bombardeando núcleos de lítio ou boro com prótons a alta velocidade.
O hélio e seus compostos
Dado que o hélio é um gás nobre, na prática não participa das reações químicas, ainda que sob a influência de descargas elétricas ou bombardeado com elétrons forma compostos com o wolfrâmio, iodo, flúor e fósforo.
Formas
O hélio líquido (hélio-4) se encontra em duas formas distintas: hélio-4 I e hélio-4 II, entre os quais ocorre uma brusca transição a 2.1768 K (ponto lambda). O He-I, acima dessa temperatura é um líquido normal, porém o He-II abaixo dessa temperatura, não se parece a nenhuma outra substância, converte-se num superfluido cujas características incomuns se devem a efeitos quânticos, um dos primeiros casos que se tem observado em escala macroscópica.
O hélio-II tem uma viscosidade nula, fluindo com facilidade através de finíssimos capilares através dos quais o hélio-I não consegue fluir, e tem, além disso, uma condutibilidade térmica muito maior que qualquer outra substância.
Isótopos
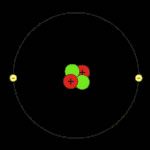
Isótopo estável He-4
O isótopo mais comum do hélio é o 4He, cujo núcleo está constituído por dois prótons e dois nêutrons. Sua excepcional estabilidade nuclear se deve ao fato de que tem um número mágico de núcleons, isto é, uma quantidade que se distribui em níveis completos (de modo análogo como se distribuem os elétrons nos orbitais). Numerosos núcleos pesados se desintegram emitindo um núcleo de 4He; este processo, que se denomina desintegração alfa – por isso o núcleo emitido se chama partícula alfa – é a origem da maioria do hélio terrestre.
O hélio tem um segundo isótopo, o 3He, além de outros mais pesados que são radioativos. O hélio-3 é praticamente inexistente na terra, dado que a desintegração alfa produz exclusivamente núcleos de hélio-4 e tanto estes como o hélio atmosférico escapam ao espaço em períodos geológicos relativamente curtos. O hélio-3 pode ocorrer associado com depósitos de hidrocarbonetos (gás natural, petróleo) cuja origem é oriunda do manto da terra.
Ambos isótopos foram produzidos durante o Big bang em quantidades significativas, e continuam sendo produzidos mediante a fusão do hidrogênio nas estrelas.
Precauções ao usar hélio
Os depósitos de gás hélio de 5 a 10 K deve ser armazenado como líquido devido ao grande incremento de pressão que se produz ao aquecer o gás a temperatura ambiente.
Quando aspirado, o hélio distorce a voz (343m/s). Deve-se tomar cuidado ao fazer isso, pois apesar de não ser tóxico, o gás hélio pode provocar sufocamento por supressão de oxigênio.
Dirigível a Hélio, da Goodyear efetuando um pouso.
